Фізика 10 клас

2024-2025 навчальний рік.
(роботи виконуємо в робочих зошитах)
5 квітня 2025 р.
ТЕМА Перший закон термодинаміки . Адіабатний процес.
теплоти Q, переданої системі або переданої системою навколишнім тілам у процесі теплообміну:
Кількість теплоти
| Ізохорний процес ( | Ізотермічний процес ( | Ізобарний процес ( |
| У ході цього процесу об’єм газу не змінюється і газ роботу не виконує, тому рівняння першого закону термодинаміки має вигляд: При ізохорному процесі вся передана газу кількість теплоти витрачається на збільшення внутрішньої енергії газу. Якщо газ ідеальний одноатомний, то кількість теплоти, передана газу, дорівнює: | У ході цього процесу температура, а отже, і внутрішня енергія газу не змінюються тому рівняння першого закону термодинаміки має вигляд: При ізотермічному процесі вся передана газу кількість теплоти йде на виконання механічної роботи. | У ході цього процесу виконується робота і змінюється внутрішня енергія газу, тому рівняння першого закону термодинаміки має вигляд: |
Задача 2.1
При швидкому стисканні m = 4 г гелію (М = 4 г/моль) в циліндрі під поршнем газ нагрівається від t1 = 7 °C до t2 = 87 °C.
Визначити
·роботу A стискання газу.
Дано: m = 4·10–3 кг М = 4 кг/кмоль t1 = 280 К t2 = 360 К |
A - ? |
Розв’язання
Через швидкоплинність процесу теплообміном газу із навколишніми тілами можна знехтувати й уважати процес адіабатним (див. п. 2.2). Отже, робота стискання А йде тільки на зміну внутрішньої енергії U, котра визначається формулою (2.1):
.
Обчислення дають
А ≈ 1,0 кДж.
ДОДОМУ- П. 38, впр. 38 (1-2). Зап. ст.227.
21 березня 2025 р.
УРОК 78
РОБОТА В ТЕМОДИНАМІЦІ


ДОДОМУ- П. 37, Зап. ст. 220 , впр. 37 (1-2)
19 березня
Урок 77
Тема- Внутрішня енергія. Способи зміни внутрішньої енергії.
Пройдіть тестування з теми.
Розділ фізики, що вивчає співвідношення і перетворення теплової та інших форм енергії
Сума кінетичних енергій хаотичного (теплового) руху частинок речовини (атомів, молекул, йонів), з яких складається тіло, і потенціальних енергій їх взаємодії
Як позначають внутрішню енергію і яка одиниця вимірювання
Процес зміни внутрішньої енергії тіла або частин тіла без виконання роботи
Укажіть види теплопередачі
Вид теплопередачі, який зумовлений хаотичним рухом частинок речовини та не супроводжується перенесенням цієї речовини
Вид теплопередачі, за якого тепло переноситься потоками рідини або газу
Вид теплопередачі, за якого енергія передається за допомогою електромагнітних хвиль
Укажіть властивості для внутрішньої енергії
фізична величина, що дорівнює енергії, яку тіло одержує (або віддає) в ході теплопередачі
Кількість теплоти, яка поглинається при нагріванні речовини (або виділяється при її охолодженні):
Знайдіть внутрішню енергію 2 кмоль ідеального одноатомного газу, взятих за температури 300 К
Додому- П.36 впр.36 (3)
17 березня
Урок 76
Внутрішня енергія. Способи зміни внутрішньої енергії.
- кінетичну енергію хаотичного (теплового) руху частинок речовини
(атомів, молекул, йонів); - потенціальну енергію взаємодії частинок речовини;енергію взаємодії атомів у молекулах (хімічну енергію);
- енергію взаємодії електронів і ядра в атомі (внутрішньоатомну енергію);
- енергію взаємодії нуклонів у ядрі (внутрішньоядерну енергію).
Внутрішню енергію позначають символом
- Атоми і молекули ідеального газу практично не взаємодіють між собою, тому внутрішня енергія ідеального газу дорівнює кінетичній енергії поступального та обертального рухів його частинок.
- Внутрішня енергія даної маси ідеального газу прямо пропорційна його абсолютній температурі.
- Внутрішня енергія — функція стану системи, тобто вона однозначно визначається основними макроскопічними параметрами (p, V, T), що характеризують систему, і незалежно від того, яким чином систему переведено з одного стану в інший, зміна внутрішньої енергії буде однаковою.
- Внутрішню енергію можна змінити двома способами: виконанням роботи і теплопередачею
Процес теплопередачі можливий тільки в разі наявності різниці температур. Довільно внутрішня енергія завжди передається від більш нагрітого тіла до менш нагрітого. Чим більша різниця температур, тим швидше(за інших рівних умов) відбувається процес передачі тепла. Існують
- Теплопровідність. Вид теплопередачі, який зумовлений хаотичним рухом частинок речовини та не супроводжується перенесенням цієї речовини. Найкращими провідниками тепла є метали, погано проводять тепло дерево, скло, шкіра, рідини (крім рідких металів); найгірші провідники тепла — гази. Передача енергії від гарячої води до батареї опалення, від поверхні води до її нижніх шарів тощо відбувається завдяки теплопровідності.

2.2.2. Приклади розв’язування задач
1. Тіло масою 5кг падає з висоти 3м. На скільки збільшиться внутрішня енергія тіла (втрату енергії в навколишньому середовищі до уваги не брати)?
Розв’язання:
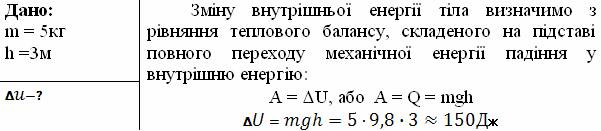
Відповідь: внутрішня енергія збільшилася на 150Дж.
2. Газ, який займає об’єм 20л за нормальних умов, було ізобарно нагріто до 800С. Визначити роботу розширення газу.
Розв’язання:

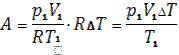
Робота розширення газу: А = ![]()
Відповідь: А = 590 Дж.
Коментарі
Дописати коментар